Molecular Therapyに掲載された論文から
レプリコンワクチン (自己増殖型mRNAワクチン) は体内で自己増殖するワクチンです。そしてRNA複製には修復の機構が無いため、増殖の際には変異が起こります。それに加え懸念となるのは、レプリコンワクチンと野生のウイルスとの間で組換えが起こり、本来存在しなかったはずの新規ウイルスを生み出す事です。
2024年8月にオランダとオーストラリアの国際的共同研究により、レプリコンワクチンと野生のウイルスが組換えを起こし得る事が報告されました。
Safety concern of recombination between self-amplifying mRNA vaccines and viruses is mitigated in vivo
Hick et al. (2024) Molecular Therapy
https://www.cell.com/molecular-therapy-family/molecular-therapy/fulltext/S1525-0016(24)00401-5
自己増殖型mRNAワクチンとウイルスの間で組換えが起こるが、安全性への懸念はin vivoでは減少する
自己増殖型mRNA (SAM) ワクチンは、疾病の発生時に迅速に導入する事ができる。正当な安全性の懸念は、アルファウイルスベースのSAMワクチンと循環しているウイルスとの間の組換えの可能性である。この理論的なリスクは、SAMワクチンの承認プロセスにおいて評価される必要がある。ここでは、in vitroおよびin vivoの広範な評価を行い、SAMワクチンと幅広い種類のアルファウイルスおよびコロナウイルスとの間の組換えを検討した。SAMワクチンは、スーパーインフェクションの排除によりアルファウイルスの共感染を効果的に制限する事が分かったが、それでも若干の共複製が可能であった。高感度細胞ベースアッセイを用いて、稀ではあるが再現可能なRNA組換え事象の結果として、複製能力のあるアルファウイルスキメラがin vitroで生成された。このキメラでは細胞培養への適応度は増加しなかった。C57BL/6Jマウス、Rag1-/-マウス、Ifnar-/-マウスでは、同じ組織内で高レベルのSAMワクチンとアルファウイルスが共複製され、生体内で生存可能なアルファウイルスキメラは検出されなかった。さらに、SAMスパイクワクチンと豚コロナウイルスの組換えは観察されなかった。結論として、SAMワクチンのアルファウイルスとの組換え能力は、環境安全性の懸念とみなされるかもしれないが、いくつかの重要な因子が、SAMワクチン接種者からのin vivoでのキメラウイルスの出現を実質的に緩和する事を述べる。
アルファウイルスにおいては、1つのウイルスによる先行感染が類似のウイルスによる後続感染を阻止する「スーパーインフェクション排除」という現象が知られています。では、レプリコンワクチンと野生のアルファウイルスが同時に細胞内で複製される事はないのでしょうか?
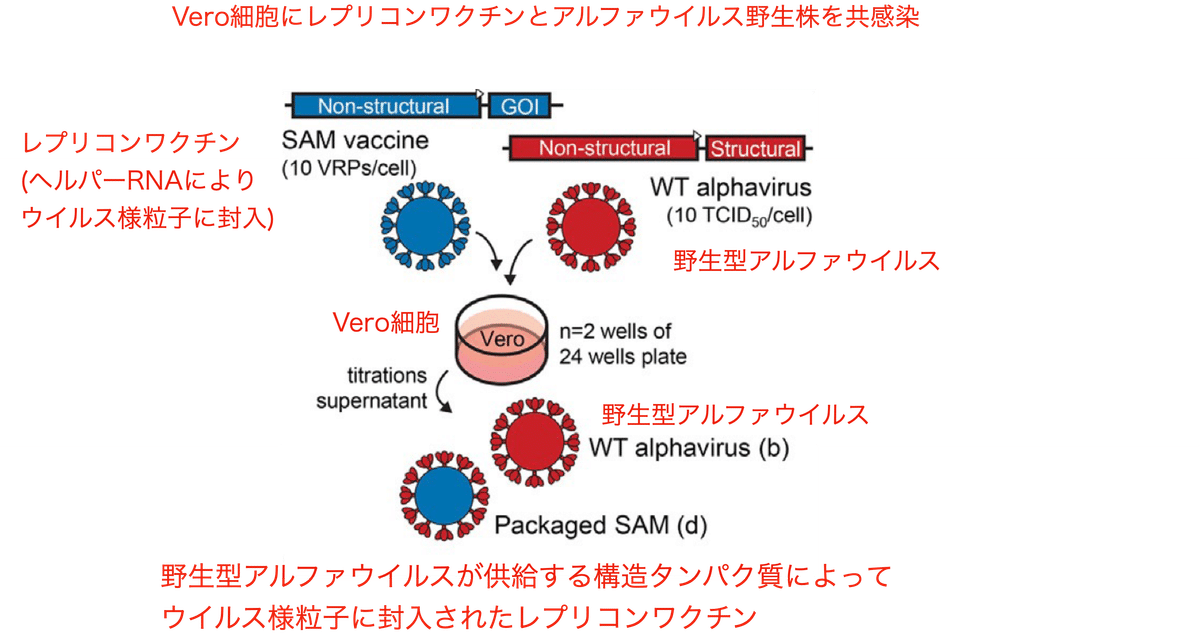
RNAゲノムにウイルスの構造タンパク質を別途供給する事で自発的にウイルスに似た構造を形成したものがウイルス様粒子です。論文内ではウイルス様レプリコン粒子 (virus-like replicon particle, VRP) と呼ばれていますが、この記事ではウイルス様粒子と表記させていただきます。筆者らはウイルス様粒子に封入したレプリコンワクチンをVero細胞に導入し、さらに野生型アルファウイルスを感染させました (図1)。今回使われたレプリコンワクチンにはレポーターとしてmCherry (赤色蛍光タンパク質) 遺伝子が含まれています。ちなみにmCherryは抗原として使われているわけではありませんので、正確には「ワクチン」ではないのですが、論文内ではレプリコンワクチンと呼んでいますので、この記事内でも踏襲します。
レプリコンワクチンとアルファウイルスへの感染が同時に起こった場合には、細胞が産生するアルファウイルスの力価は大きく低下しましたが、アルファウイルスがレプリコンワクチンの前に加えられた場合にはウイルスの力価の低下はわずかでした。そしてレプリコンワクチンにコードされたmCherryレポーターがほとんどの細胞で強く発現されました。このように、レプリコンワクチンは過剰感染を減少させはするものの、ウイルスの感染自体を排除する事はできませんでした。
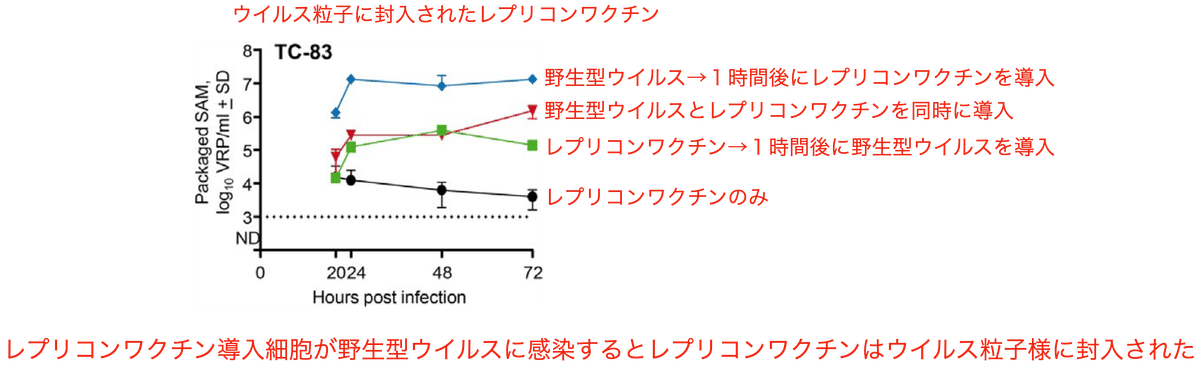
さらに共感染/形質転換されたVero細胞の上清からは、ウイルス様粒子に封入されたレプリコンワクチンが検出されました (図2)。これは、野生型アルファウイルスが構造タンパク質を供給した事によってレプリコンワクチンがウイルス様粒子に取り込まれた事を意味します。ウイルス様粒子に封入されたレプリコンワクチンはウイルス同様に感染性を持ちます。レプリコンワクチンのウイルス様粒子への取り込みは、野生型アルファウイルス感染の1時間後にレプリコンワクチンを導入した場合に高い効率で起こりました。
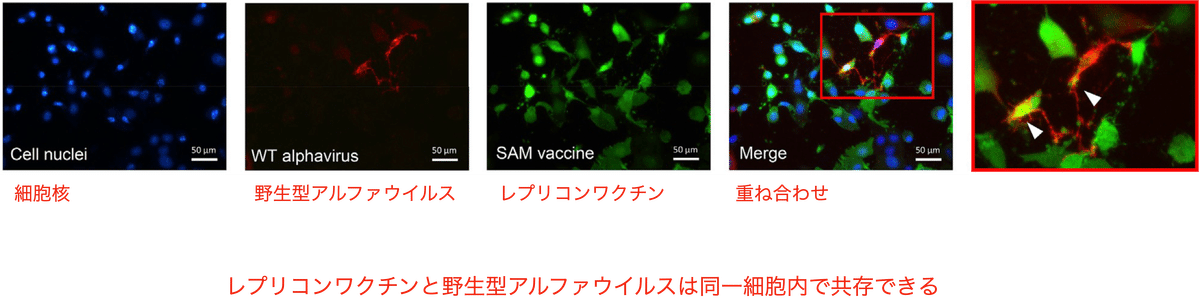
蛍光顕微鏡による観察では、7%の細胞でレプリコンワクチンと野生型アルファウイルスが共存していました (図3)。こうした実験結果からも分かるように、レプリコンワクチンと野生型アルファウイルスは同一細胞内で同時に複製される場合があり、その効率は野生型アルファウイルスの感染のタイミングに依存します。そしてレプリコンワクチンのデザインによっては「ウイルス化した」レプリコンワクチン粒子も生じやすくなります。
著者らはキメラウイルスのスクリーニングに遺伝子ノックアウト細胞を利用しました。この細胞はHeLa GTPase活性化タンパク (SH3ドメイン) 結合タンパクノックアウト細胞 (DG3BP細胞) です。今回の実験で使われた12種類のアルファウイルスのうちベネズエラウマ脳炎ウイルス、ベバルウイルス、セムリキ森林ウイルスの3種類のウイルスがHeLa DG3BP細胞で複製されましたが、残りの9種類は複製されませんでした。ここで使われたベネズエラウマ脳炎ウイルスはワクチン株「TC-83」です。
増殖しなかった9種類のアルファウイルスをVero細胞に感染させ、その1時間後にTC-83由来のレプリコンワクチンが導入されました。キメラアルファウイルスの生成は、共同感染/形質転換させたVero細胞からの上清をHeLa細胞およびDG3BP細胞に移し、細胞障害性で評価されました。生存可能なキメラウイルスは双方に由来する生存に必須な領域 (TC-83のnsP3-超可変ドメイン (G3BP非依存性) と野生型アルファウイルスの構造タンパク質) を取り込んでいるはずです。
レプリコンワクチンと9種類のウイルスのそれぞれを共感染させたところ、9つのうちゲタウイルスでのみ細胞障害性が実験2回中1回観察されました。次にゲタウイルスにのみ焦点を絞ってレプリコンワクチンと共感染させると、細胞障害性は96回中1回観察されました。 最初の実験でのレポーター遺伝子はmCherry、2回目の実験でのレポーター遺伝子はナノルシフェラーゼです。
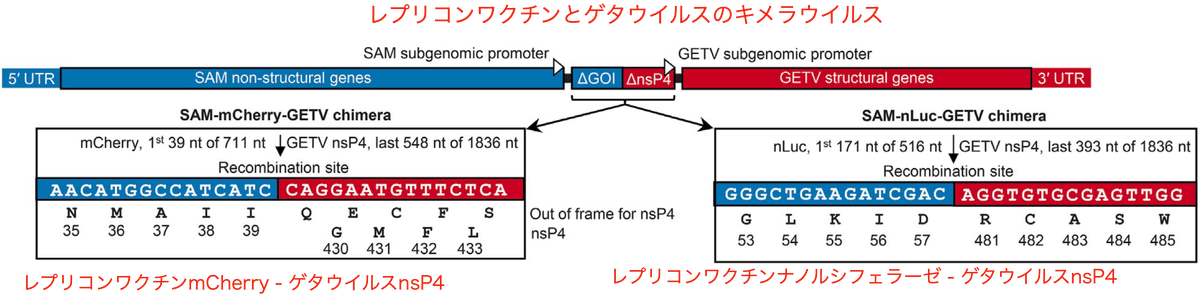
RNA-seq法により培養上清のRNAの配列を解析すると、両キメラはレプリコンワクチン内のmCherryやナノルシフェラーゼとゲタウイルス内のnsP4遺伝子内で組換えを起こしている事が確認されました (図4)。レプリコンワクチンとゲタウイルスのサブゲノムプロモーターは保持されており、非翻訳領域は両者のものを含んでいました。
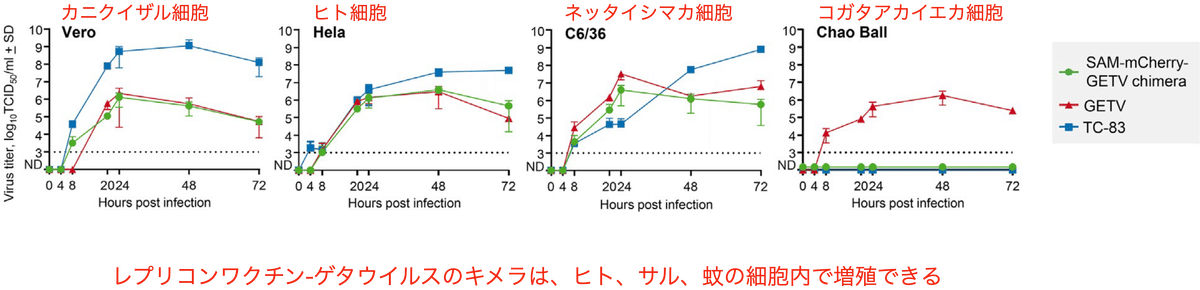
キメラウイルス (レプリコン-mCherry/GETVキメラ) は、カニクイザル細胞 (Vero) のみならずヒト細胞 (Hela) やネッタイシマカ細胞 (C6/36) でも増殖する事ができました (図5)。キメラウイルスの力価はTC-83やゲタウイルスと比較すると低かったのですが、これは組換えウイルスのプロモーターなどが最適ではなかった可能性があります。

さて、この論文を踏まえ、改めて私自身で組換え点を詳細に解析してみました (図6)。その結果、意外にも組換えRNA同士には相同性がありませんでした。つまりこれは遺伝子間に相同性がなくとも組換えが起こるという事の証明であり、レプリコンワクチンは潜在的にどのウイルスとも、また細胞内のどのRNAとも組換えが起きる可能性を示唆します。また遺伝子組換えの機序からも、近縁のウイルスとの間ではさらに組換えの頻度が上がるでしょう。
マウスの実験では生体内で生存可能なアルファウイルスキメラは検出されませんでした。しかしこれは実験室内のごく小スケールでのマウスを使った実験の話です。この結果のみをもってレプリコンワクチン接種が人間社会で拡大した場合のin vivoでの組換えや病原性のリスクを正確に評価する事は不可能です。
もともとアルファウイルスRNAは様々なケースで組換えが可能である事が知られています。例えば西部ウマ脳炎ウイルスは、古代に東部ウマ脳炎様ウイルスとシンドビス様ウイルスとの間に起こった組換えから発生したと考えられています。またブラジルとハイチからはマヤロウイルスの組換え体の発見が報告されており、チクングニアウイルス分岐群間の組換えも示唆されています。また多くのin vitroおよびin vivoの研究においても、ウイルス様粒子の製造中にアルファウイルスの鋳型が組換えを起こす傾向がある事が示されています。こうした事実を踏まえても、レプリコンワクチンが野生型アルファウイルスと組換えを起こして新規キメラウイルスが生成される可能性が否定できません。
そしてもう一つの重大な懸念事項はレプリコンワクチンの個体間伝播です。人体は閉鎖系ではありません。人体は恒常性を保つために、取り込んだ有害物質を代謝産物として、あるいはそのままの形で体外に排出しようとします。例えば抗癌剤治療を受けている人の近親者が抗癌剤に暴露する事例などもよく知られています。レプリコンワクチン接種者は受け取ったレプリコンワクチンを体内で全て分解できるとは限りません。排泄物、嘔吐物などを介して近親者に暴露させる可能性もあれば、呼気や汗に含まれるエクソソームなどを介して周囲に放出する可能性もあります。また、蚊を介して血液から血液へと直接的に他者に受け渡される恐れもあるでしょう。
この論文が示唆する他のリスクとしては、ウイルス感染によってレプリコンワクチンがウイルス様粒子内に取り込まれる経路の存在です。このリスクはレプリコンワクチンがアルファウイルスのパッケージングシグナルを含んでいる場合にはさらに高くなります。なぜならパッケージングシグナルとはウイルスゲノムをウイルス粒子に「配達するための荷札 (タグ)」の様なものだからです。つまりレプリコンワクチンを接種した者がアルファウイルスに感染した場合にはレプリコンワクチンがウイルス粒子内に取り込まれる可能性があるという事です。ウイルス様粒子はエクソソームよりもさらに感染性と伝染力が高いため、ウイルス様レプリコンワクチン粒子が他者に感染する懸念が払拭できません。
実験結果が示すものはまさに「レプリコンワクチンのウイルス化」の実例であり、レプリコンワクチンが野生のアルファウイルスから殻 (構造タンパク質) の遺伝子を盗んでウイルス化したと言えるものです。
本来脳内は免疫の働きが弱く、脳に炎症を起こすアルファウイルスは危険なウイルスです。実際、ベネズエラウマ脳炎ウイルスは脳炎などの重篤な症状を引き起こします。レプリコンワクチンと野生のウイルスとのキメラウイルスは人体に深刻な影響をもたらす可能性があります。さらにこうした組換えは病原性のある新規のウイルスを進化させ得るものであり、環境に対する重大なリスクである事を想定する必要があります。



コメント